Los grupos de investigación de los investigadores del Centro Nacional de Biotecnología del CSIC, Luis Enjuanes y José María Casasnovas, han descifrado cómo el sistema inmune puede prevenir infecciones de coronavirus.
 Los coronavirus provocan importantes enfermedades respiratorias e intestinales, como resfriados y el síndrome respiratorio agudo (SARS). El trabajo, que aparece en la revista PLOS Pathogens, muestra que los anticuerpos previenen la unión de los coronavirus a proteínas de la superficie celular conocidas como receptores, aportando una información fundamental para el desarrollo de vacunas que prevengan las infecciones por coronavirus.
Los coronavirus provocan importantes enfermedades respiratorias e intestinales, como resfriados y el síndrome respiratorio agudo (SARS). El trabajo, que aparece en la revista PLOS Pathogens, muestra que los anticuerpos previenen la unión de los coronavirus a proteínas de la superficie celular conocidas como receptores, aportando una información fundamental para el desarrollo de vacunas que prevengan las infecciones por coronavirus.
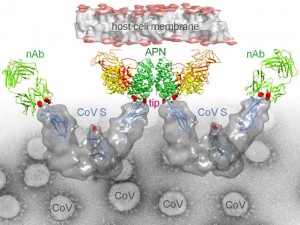
La llamada proteína S, presente en la envuelta de los coronavirus, se encarga de la unión del virus a receptores que se encuentran en la superficie de la célula, hecho con el que da comienzo la infección. Los investigadores han logrado fotografiar la estructura de la unión de la proteína S a una proteína celular conocida como aminopeptidasa N, que es receptor para un grupo amplio de coronavirus. La estructura identifica la región (“tip”) de la proteína S que acopla el virus a la célula para iniciar la infección. Este “tip” encaja en dos hendiduras de la aminopeptidasa N.
El trabajo va más allá, mostrando que este “tip” es diana de anticuerpos que neutralizan la infección de coronavirus. Con objeto de escapar de esta presión inmunológica, este “tip” parece evolucionar en los coronavirus, lo que en ciertos casos obliga a estos virus a seleccionar receptores celulares distintos para poder iniciar la infección celular. No obstante, el “tip” parece ser el “talón de aquiles” de un grupo amplio de estos virus. El trabajo también presenta otra novedad relevante, al mostrar la primera estructura descrita para un aminopeptidasa N, proteína de la superficie celular que se ha implicado en multitud de funciones celulares, así como una diana relevante para el tratamiento de tumores. La aminopeptidasa N es un enzima que está implicada en procesos de angiogénesis y motilidad celular, necesarios para el crecimiento y metástasis de tumores. Se han desarrollado numerosos fármacos que inhiben la función enzimática de este enzima y previenen el desarrollo de tumores, algunos de los cuales están en ensayos clínicos en la actualidad. El conocimiento de la estructura de la aminopeptidasa N y de complejos con fármacos, que los grupos del CSIC están analizando en la actualidad, abre la puerta al diseño de nuevas drogas para el tratamiento del cáncer.
Según los investigadores del CSIC, “el haber podido identificar las zonas implicadas en la unión al receptor, así como mostrado que pueden ser diana de anticuerpos neutralizantes, indica el camino a seguir para el desarrollo de vacunas que prevengan infecciones de coronavirus. El objetivo es enfocar la respuesta inmunitaria hacia el “tip” de la proteína S con inmunógenos recombinantes. Durante la infección viral o mediante la administración de virus inactivados en vacunas, nuestro sistema inmune genera una extensa variedad de anticuerpos contra diversas regiones de las proteínas virales, muchos de los cuales no previenen la infección. Con objeto de bloquear la infección, debemos de educar a nuestro sistema inmune para que genere, preferencialmente, anticuerpos conocidos como neutralizantes, que son capaces de prevenir la infección viral. En el caso de los coronavirus, resulta obvio hacia donde debemos de enfocar esta respuesta, lo que requerirá el diseño de proteínas recombinantes similares a las usadas en este estudio.
Cita: Juan Reguera, César Santiago, Gaurav Mudgal, Desiderio Ordoño, Luis Enjuanes and José M Casasnovas. Structural bases of coronavirus attachment to host aminopeptidase N and its inhibition by neutralizing antibodies. PLOS Pathogens, 8(8): e1002859. doi:10.1371/journal.ppat.1002859.r
Fuente: www.cnb.csic.es






